
Д-димер: диагностическое значение теста в диагностике венозных тромбоэмболий
- Категория: Новости
Носко Игорь Владимирович
врач-анестезиолог-реаниматолог
Венозная тромбоэмболия (ВТЭ) – это одна из важных медицинских проблем во всем мире. ВТЭ включает тромбозы глубоких вен нижних конечностей (ТГВ), которые часто приводят к тромбоэмболии легочной артерии (ТЭЛА). ТЭЛА часто становится причиной острой сердечной недостаточности и смерти больного. В общей популяции на 100 000 населения ежегодно фиксируется 50-70 новых случаев ТГВ. В пожилом и старческом возрасте частота ТГВ увеличивается в несколько раз (до 200 случаев на 100 000 населения в год). Легочную эмболию регистрируют ежегодно с частотой 35-40 на 100 000 человек (1). Смертность от ТЭЛА занимает третье место после ИМ и инсульта (3). Распространенность ВТЭ постепенно увеличивается с возрастом и достигает к 55-64 годам – 500 случаев на 100000 населения, а к 75-84 годам – 1564 случаев на 100000 человек.
Преобладающими факторами риска ВТЭ в пожилом возрасте являются: малая подвижность, онкологические заболевания, сопутствующие заболевания (в особенности сердечная недостаточность, инсульт, хроническая обструктивная болезнь легких, диабет и другие хронические заболевания), а также снижение мышечного тонуса, хрупкость костей, венозная недостаточность, заместительная гормональная терапия у женщин и повышенные уровни некоторых протромботических факторов (например, фибриногена, фактора VII, фактора VIII и гомоцистеина) (2).
Вопрос диагностики ТЭЛА актуален из-за тяжести заболевания и высокой летальности. Очень часто ТЭЛА развивается молниеносно и нет времени на диагностику.
Смертность в течение 1 часа составляет 65%, а через 2,5 часа – 80%. Однако при своевременной диагностике и ранней правильной терапии количество неблагоприятных исходов снижается и составляет не более 10% (4).
Диагноз ТГВ и ТЭЛА устанавливается не только на основании клинических признаков, но и на основании объективных данных, полученных с помощью инструментальных исследований. «Золотым стандартом» в диагностике ТЭЛА является КТ ангиография легочных сосудов с контрастированием. При диагностике ТГВ - ультразвуковое компрессионное дуплексное ангиосканирование .
Использование визуализационных методов имеет ряд существенных ограничений. Прежде всего, это их высокая стоимость, а также сниженная доступность в неотложных ситуациях, потенциальный вред для здоровья пациентов, при использовании ионизирующей радиации и йодированных контрастных агентов, провоцирующих развитие нефропатии .
В целом, согласно данным международных исследований, после проведения инструментальной диагностики диагноз ТЭЛА подтверждается только у 15-25% пациентов (7). Перед проведением инструментальных исследований пациенты нуждаются в объективном лабораторном тесте для подтверждения или исключении диагноза. В настоящее время таким наиболее приемлемым и эффективным исследованием для пациентов с подозрением на ТЭЛА является тест на Д-димер (3).
Д-димер представляет собой фрагменты молекулы фибрина, образующиеся при его распаде (протеолитической деградации) под действием активного плазмина (8). Наличие в плазме крови Д-димера свидетельствует об образовании и деградации фибринового сгустка внутри сосудистого русла и отражает активацию как гемостаза, так и фибринолиза (9). Процесс образования Д-димера состоит из нескольких этапов, это: 1) протеолитическая деградация фибриногена под действием тромбина, отщепление от него фибринопептидов А и В и образование фибрин-мономеров; 2) самопроизвольная полимеризация фибрин-мономеров в растворимый фибрин-полимер; 3) стабилизация растворимого фибрин-полимера в нерастворимый тромб под действием фактора XIII, образующего ковалентные связи («поперечные сшивки») между находящимися рядом D-доменами фибрин-мономеров в присутствии ионов Ca2+ ; 4) деградация нерастворимого поперечно-сшитого фибрина под действием активного плазмина (8,10). Действие фибринолитической системы направлено на лизис фибрина, а при чрезмерной активации – и фибриногена. В результате образуется смесь продуктов деградации фибрина/фибриногена (ПДФ) (рис.1).
Рис.1 Образование и распад фибрина (10).
Продуктами деградации фибрина (полимерной молекулы) являются более крупные фрагменты - Д-димеры, тримеры и другие вещества, содержащие ковалентные D-D связи, не разрушаемые плазмином, тогда как в результате лизиса фибриногена образуются мономерные формы D и E доменов фибрина. Следовательно, только продукты деградации поперечно-сшитого фибрина содержат Д-димеры (3).
Концентрация измеряемого Д-димера в плазме зависит от размера и возраста тромба. Повышение Д-димера в плазме наблюдается примерно через 2 ч после начала тромбоза (7). Д-димер метаболизируется в почках, время его полу-жизни при сохранной функции почек составляет приблизительно 6-8 часов (10).
Д-димер – чувствительный, но не специфичный маркер тромбозов: исключает, но не подтверждает тромбоз.
Д-димер считается биохимическим «золотым стандартом» для диагностики пациентов с подозрением на ВТЭ (9). Диагностическое значение Д-димера основывается на его высокой чувствительности и, следовательно, способности исключать ВТЭ, если его концентрация в плазме меньше определенной пороговой величины (cut-off) поэтому Д-димер обладает высоким отрицательным предиктивным значением (>98%). При этом его положительное предиктивное значение для диагностики ВТЭ весьма низкое (≤15%), поскольку уровень Д-димера повышается и по многим другим причинам.
Другие причины для увеличения Д-димера:
- фибринолитическая терапия в предшествующие 7 дней,
- травма или хирургия (в течение 4 недель после),
- диссеминированное внутрисосудистое свертывание (ДВС),
- инфаркт миокарда,
- атеросклероз,
- сепсис,
- тяжелые инфекции,
- цирроз печени,
- злокачественные опухоли,
- беременность
- пожилой возраст (старше 60 лет) (7).
Поэтому пациенты с повышенным уровнем Д-димера нуждаются в инструментальном обследовании для подтверждения или исключения диагноза тромбоза глубоких вен или ТЭЛА. Основное диагностическое значение Д-димера – исключение наличия тромбозов в сосудистом русле при дифференциальной диагностике ТГВ, ТЭЛА и другой тромботической патологии (8).
Поскольку измерение Д-димера связано с диагностикой опасных для жизни патологий (например, ТЭЛА), то в экстренных случаях важными условиями являются: быстрое получение результата, сокращение времени на преаналитический этап за счет исследования цельной венозной крови сразу после взятия, а также возможность круглосуточного измерения единичных проб. Поэтому в экспресс-лабораториях широко используются «методы диагностики у постели больного» (Point-of-care testing).
Однако низкая специфичность теста на Д-димер является причиной того, что он не может быть использован как единственным рутинный тест для диагностики ВТЭ, особенно для госпитализированных пациентов. Больным без каких-либо клинических признаков, позволяющих предположить наличие ТГВ, проводить определение Д-димера с целью скрининга не следует (1). Д-димер – это так называемый тест второй линии, который проводится только после предварительной клинической оценки вероятности развития ВТЭ. По мнению экспертов (6) оценка клинической картины заболевания является первичным этапом, от которого зависит дальнейшая диагностическая стратегия и интерпретация результатов. При подозрении на наличие ВТЭ пациентов классифицируют в соответствии с валидированными клиническими шкалами, чаще всего это шкала Уэллса или Женевский алгоритм (5, 7), Таблицы 1 и 2. Важно отметить, что шкала Уэллса применяется как для амбулаторных, так и для госпитализированных пациентов, тогда как Женевский алгоритм – только для амбулаторных пациентов (6). Для оценки клинической вероятности ТГВ и ТЭЛА можно применять две альтернативные схемы: трехуровневую (клиническая вероятность низкая, промежуточная или высокая) или двухуровневую (например, ТЭЛА маловероятна или вероятна).
Таблица 1. Шкала Уэллса для оценки вероятности ТГВ (7).
|
Клинический признак |
Баллы |
|
Активный рак (в настоящее время или в предшествующие 6 месяцев) |
+1 |
|
Плегия/парез, недавнее наложение гипса на нижние конечности |
+1 |
|
Постельный режим > 3 суток или крупная операция в предыдущие 12 недель |
+1 |
|
Болезненность при пальпации по ходу глубоких вен |
+1 |
|
Отек всей ноги |
+1 |
|
Разница в отеке икр >3 см по сравнению с асимптоматической конечностью (измеренная на 10 см ниже большеберцовой бугристости) |
+1 |
|
Отек с ямкой на больной ноге |
+1 |
|
Расширенные коллатеральные поверхностные вены (не варикоз) |
+1 |
|
ТГВ в анамнезе |
+1 |
|
Другой диагноз как минимум столь же вероятен |
-2 |
|
Клиническая вероятность (3 уровня) |
|
|
Низкая (~3%) |
<1 |
|
Средняя (~17%) |
1-2 |
|
Высокая (~75%) |
>2 |
|
Клиническая вероятность (2 уровня) |
|
|
ТГВ маловероятен |
≤1 |
|
ТГВ вероятен |
≥2 |
Таблица 2. Клинические алгоритмы оценки вероятности ТЭЛА (5).
|
Пересмотренный женевский алгоритм [ |
Шкала Уэллса |
||
|
Показатели |
Баллы |
Показатели |
Баллы |
|
Факторы риска Возраст старше 65 лет ТГВ или ТЭЛА в анамнезе Операция или перелом в течение 1 мес. Злокачественная опухоль |
+1 +3 +2 +2 |
Факторы риска ТГВ или ТЭЛА в анамнезе Операция или иммобилизация Рак |
+15 +15 +1 |
|
Симптомы Боль в одной нижней конечности Кровохарканье |
+3 +2 |
Симптомы Кровохарканье |
+1 |
|
Физические данные Частота сердечных сокращений 75-94 в минуту ≥95 в минуту Боль в ноге при пальпации или односторонний отек |
+3 +5 +4 |
Физические данные Частота сердечных сокращений >100 в минуту Признаки ТГВ |
+15 +3 |
|
Клиническая оценка Альтернативный диагноз менее вероятен, чем диагноз ТЭЛА |
+3 |
||
|
Клиническая вероятность Низкая Средняя Высокая |
Сумма 0-3 4-10 ≥11 |
Клиническая вероятность (3 уровня) Низкая Средняя Высокая |
Сумма 0-1 2-6 ≥7 |
|
Клиническая вероятность (2 уровня) ТЭЛА маловероятна 0-4 ТЭЛА вероятна >4 |
|||
Количественное определение Д-димера для исключения ВТЭ рекомендуется проводить только у амбулаторных/экстренно госпитализированных пациентов с низким или промежуточным риском (для ТГВ <2 по шкале Уэллса, для ТЭЛА <10 по Женевской шкале или <6 по шкале Уэллса). Пациентов с высоким риском ТГВ и ТЭЛА необходимо сразу направлять на инструментальное обследование без предварительного определения Д-димера (5,7).
Алгоритм диагностики ВТЭ у пациентов с низким или промежуточным риском
Сначала определяется клиническая вероятность развития ВТЭ, ТЭЛА, а затем определяется уровень Д-димера. В этих условиях значения теста повышается.
Рис. 2. Алгоритм диагностики ВТЭ и использованием оценки клинической вероятности, Д-димера и методов визуализации (7).
Диагностическая стратегия, основанная на совместном использовании шкалы пре-тестовой оценки клинической вероятности и Д-димера, увеличивает эффективность диагностики пациентов с подозрением на ВТЭ, даёт возможность исключить ТЭЛА примерно у 30% пациентов в ОНП с трёхмесячным риском тромбоэмболии у оставленных без лечения пациентов на уровне <1% (5) и позволяет снизить количество дорогостоящих и небезопасных для здоровья пациентов процедур (7).
Заключение.
Таким образом, диагностический алгоритм, основанный на совместном использовании шкал определения клинической вероятности ВТЭ, ТЭЛА и порога Д-димера значительно увеличивает специфичность диагностики ВТЭ без потери ее чувствительности.
Номер Литература References
1 Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений. Москва, издательство «Планида», 2014
2 Lippi G, Favaloro E.J, Cervellin G. A Review of the Value of D-dimer Testing for Prediction of Recurrent Venous Thromboembolismwith Increasing Age. Seminars in Thrombosis & Hemostasis, 2014, 40 (6), 634-639.
Doi:10.1055/s-0034-1384630. Lippi G, Favaloro E.J, Cervellin G. A Review of the Value of D-dimer Testing for Prediction of Recurrent Venous Thromboembolismwith Increasing Age. Seminars in Thrombosis & Hemostasis, 2014, 40 (6), 634-639.
Doi:10.1055/s-0034-1384630.
3 Кишкун А.А.. Лабораторная диагностика неотложных состояний. Лабора, Москва, 2012:271-279.
4. Wan S. Thrombolysis for high-risk PE: Meta-analysis Studies that included patients with high-risk PE. Chest 1995; 108(4), 978-981
doi:10.1378/chest.108.4.978 Wan S. Thrombolysis for high-risk PE: Meta-analysis Studies that included patients with high-risk PE. Chest 1995; 108(4), 978-981
doi:10.1378/chest.108.4.978
5 Рекомендации ESC по диагностике и ведению пациентов с острой эмболией системы легочной артерии 2014. Российский кардиологический журнал 2015, № 8 (124), 67- 110.
Doi: 10.15829/1560-4071-2015-08-67-110.
6 Robert-Ebadi H, Righini M. Diagnosis and management of pulmonary embolism in the elderly. European Journal of Internal Medicine 2014, 25 (4), 343–349 doi:10.1016/j.ejim.2014.03.009 Robert-Ebadi H, Righini M. Diagnosis and management of pulmonary embolism in the elderly. European Journal of Internal Medicine 2014, 25 (4), 343–349 doi:10.1016/j.ejim.2014.03.009
7 Olson J.D, Adcock D.M, Bush T.A, de Moerloose P., Gardiner C, Giniard V.R, Grimaux M., McMahan C.A., Prihoda A., Rico-Lazarowsli A, Sales M, Stang L, Trumbull K, Van Cott E, Wissel T, Clinical and Laboratory Standards Institute (CLSI). Quantitative D-Dimer for exclusion venous thromboembolic disease. Approved Guideline. H-59A, 2011, 31 (6), 1-31.
8 Гильманов А.Ж. D-Димер: Что? Как? У кого? С какой целью? Научно-практический журнал «Клинико-лабораторный консилиум» 2009, №06 (31), 38-46 Gilmanov A. D-Dimer: Analyte, methods, targets, purposes. «Kliniko-laboratornyi konsilium » 2009 №06 (31), с. 38-46 (In Russ.)
9 Lippi G , Cervellin G, Casagranda I , Morelli B, Testa S, Tripodi A. D-dimer testing for suspected venous
thromboembolism in the emergency department. Consensus document of AcEMC, CISMEL, SIBioC, and SIMeL
Clin Chem Lab Med. 2013, 52(5), 1-8
doi 10.1515/cclm-2013-0706 Lippi G , Cervellin G, Casagranda I , Morelli B, Testa S, Tripodi A. D-dimer testing for suspected venous
thromboembolism in the emergency department. Consensus document of AcEMC, CISMEL, SIBioC, and SIMeL
Clin Chem Lab Med 2013; Clin Chem Lab Med. 2013, 52(5),1-8
doi 10.1515/cclm-2013-0706
10 Lippi G, Tripodi A, Simundic A-M. International Survey on D-Dimer Test Reporting: A Call for Standardization. Seminars in Thrombosis & Hemostasis 2015, 41 (3), 287-293
doi:10.1055/s-0035-1549092. Lippi G, Tripodi A, Simundic A-M. International Survey on D-Dimer Test Reporting: A Call for Standardization. Seminars in Thrombosis & Hemostasis 2015, 41 (3), 287-293
doi:10.1055/s-0035-1549092.
11 Методическое пособие Диакон Соловьева И.В.
27 сентября 2019 г.

Антикоагулянты, влияющие на процесс тромбообразования
- Категория: Новости
ч. 2 Целесообразность применения антикоагулянтной терапии тем или иным препаратом определяется конкретной клинической ситуацией.

Синдром Хагемана
- Категория: Новости
Анестезиолог-реаниматолог Юлия Егорова о синдроме нарушения свертывания крови, который повышает риск тромбозов и спонтанных выкидышей
Дефицит фактора Хагемана (XII фактор свертывания крови) — это редкое (около 1:1 000 000 населения) и наследственно обусловленное нарушение коагуляционного гемостаза. Наследуется этот дефект преимущественно аутосомно-рецессивно, но в единичных случаях — более тяжелых — выявляется аутосомно-доминантное наследование. В иммунологических исследованиях было показано, что синдром Хагемана характеризуется сниженным синтезом фактора Хагемана, а не образованием его аномальных молекул.
В 1954 году в Кливленде (США) гематолог Оскар Ратнов наблюдал пациента Джона Хагемана 37 лет со значительно увеличенным временем кровотечения. Обратив внимание на то, что, несмотря на изменения в коагуляции, пациент перенес хирургическую операцию без значительного кровотечения, Ратнов совместно с биохимиком Эрлом Дэйви установил, какого именно белка не хватало в плазме у этого пациента, заподозрив в этом причину нарушения свертываемости крови. Этот сложный белок и был назван фактором Хагемана, а после того как английский гематолог Роберт Макфарлан в 1964 г. сформулировал каскадную теорию гемостаза, занял в ней место как 12‑й фактор свертывания.
Кровотечение — одно из самых опасных для организма состояний, защита организма от него должна быть как надежной, так и саморегулирующейся, чтобы остановка кровотечения не переходила в распространенный тромбоз. Эту роль выполняют сразу несколько систем — клеточная (тромбоцитарный гемостаз) и сложная система белков плазмы, состоящая из многих взаимосвязанных факторов свертывания:
- I — Фибриноген
- II — Протромбин
- III — Тканевой тромбопластин
- IV — Ионы кальция
- V — Проакцелерин
- VI — Акцелерин — изъят из классификации, так как является
активированным V фактором - VII — Проконвертин
- VIII — Антигемофильный фактор
- IX — Фактор Кристмаса
- X — Фактор Стюарта—Прауэра
- XI — Плазменный предшественник тромбопластина
- XII — Фактор Хагемана
- XIII — Фибринстабилизирующий фактор
- Фактор Флетчера — плазменный прекалликреин
- Фактор Фитцжеральда — высокомолекулярный кининоген
- Фактор Виллебранда — опосредует связывание тромбоцитов с субэндотелием
Фактор Хагемана — сиалогликопротеин — сложное органическое соединение, помимо белковой части включающее в себя олигосахарид и сиаловые кислоты. Сиалогликопротеин синтезируется в печени, далее свободно и «без дела» циркулирует в плазме крови, пока не соприкоснется с отрицательно заряженными поверхностями, например, коллагеном поврежденной ткани или с калликреином, о котором стоит рассказать подробнее.
Калликреин — один из основных функциональных элементов сложной калликреин-кининовой системы, регулирующей процессы воспаления, свертывания крови, микроциркуляции и функции сосудистой стенки.
Фактор Хагемана, активированный повреждением ткани, участвует в запуске калликреин-кининовой системы, превращая прекалликреин в калликреин, а калликреин в свою очередь активирует все новые молекулы фактора Хагемана.
Получается петля для каскадного нарастания процесса. За счет этого небольшое количество поврежденных тканей вызывает реакцию в значительной части плазмы крови.
Кроме того, на 12 фактор (Хагемана) в активной форме действует 13 фактор (фибринстабилизирующий фактор), что запускает каскад биохимических реакций среди молекул, исходно присутствовавших в крови, — внутренний путь коагуляции. В отличие от внутреннего пути, внешний запускается попаданием в кровь тканевого тромбопластина из поврежденных тканей.
Таким образом, фактор Хагемана оказывается связующим звеном между процессами воспаления и свертывания крови; до его открытия связь этих процессов была гипотетической.
Клиническая картина
Клинически дефицит 12 фактора свертывания крови проявляется удлинением времени кровотечения без каких‑либо других симптомов нарушения гемостаза. Выраженность удлинения времени кровотечения зависит от типа наследования генетического дефекта. При доминантном типе дефицит выражен сильнее, при рецессивном — частично компенсируется другими факторами свертывания. Время кровотечения увеличено из‑за замедленной инициации каскадной системы свертывания крови. Склонности к патологическим кровотечениям пациенты не проявляют, поэтому заболевание часто не обнаруживают или обнаруживают случайно при лабораторном обследовании или предоперационном скрининге.
Немного парадоксальным кажется то, что при дефиците фактора свертывания проявляют себя не кровотечения, а тромбозы. Например, Джон Хагеман, по имени которого назван фактор свертывания, впоследствии погиб от тромбоэмболии, которой осложнился перелом костей таза. Современные опубликованные клинические случаи оперативных вмешательств у пациентов с синдромом Хагемана, к счастью, заканчивались благополучно. Тромбофилические нарушения связаны с тем, что XII фактор участвует в разрушении тромбов путем активации калликреин-кининовой системы. Активный калликреин не только запускает генерацию кининов, регулирующих воспаление, сосудистый тонус и болевые реакции, но и превращает неактивный белок плазминоген в активный фермент плазмин (фибринолизин), который и растворяет фибриновую часть тромба. Поэтому с дефицитом фактора Хагемана ассоциированы:
- тромбозы
- мигрирующие тромбофлебиты
- тромбоэмболии
- инфаркты
- спонтанные аборты
Диагноз и прогноз
Кроме лабораторных исследований установить диагноз помогут анамнестические данные: склонность к длительным кровотечениям и тромботическим осложнениям у пациента и его родственников, а также положительный симптом Румпеля — Лееде (появление мелкоточечных кровоизлияний дистально от наложенного на плечо жгута). Прогноз при дефиците фактора Хагемана в большинстве случаев благоприятный, лечение не требуется. Коррекции это состояние требует только в связи с хирургическими вмешательствами. В качестве подготовки к операции может быть назначено переливание небольших доз свежезамороженной плазмы.
Период выведения донорского XII фактора — 48–56 ч. Также при наличии этой коагулопатии следует уделять большее внимание профилактике тромботических осложнений: профилактическая компрессия нижних конечностей, УЗИ-контроль состояния вен нижних конечностей и малого таза, особенно при длительном постельном режиме. В послеоперационном периоде для профилактики тромбозов необходимо назначение низкомолекулярных гепаринов, а для терапии кровотечений — отказ от применения ингибиторов фибринолиза, таких как аминокапроновая и транексамовая кислота.

ГИПЕРКОАГУЛЯЦИЯ У ПАЦИЕНТОВ С КОКСАРТРОЗОМ И АНГБК ПОСЛЕ ЭНДОПРОТЕЗИРОВАНИЯ ТАЗОБЕДРЕННОГО СУСТАВА
- Категория: Новости
Калашников М.Н., Колесникова Е.Т., Семенюта В.В.
ФГБОУ ВО Ижевская государственная медицинская академия, Ижевск
Ижевск, Россия (426076, г. Ижевск, ул. Коммунаров, 281)
Источник: https://scienceforum.ru/2020/article/2018020024
Большие ортопедические операции, в том числе тотальное эндопротезирование тазобедренного сустава, относятся к оперативным вмешательствам высокого риска в отношении развития венозных тромбозов и эмболий. Известно, что при отсутствии антикоагулянтной терапии после эндопротезирования крупных суставов тромбоз глубоких вен (ТГВ) встречается в 41-85% случаев, фатальная тромбоэмболия легочной артерии (ТЭЛА) в 0,1-1% случаев [6]. Важно и то, что ТГВ или ТЭЛА могут манифестировать в течении нескольких недель после выписки из стационара [7]. Данным осложнениям предшествуют изменения лабораторных показателей крови: показатели коагулограммы чаще соответствуют гиперкоагуляции.
Двумя из наиболее часто встречающихся показаний для тотального эндопротезирования тазобедренного сустава являются перелом шейки бедреной кости, коксартроз и асептический некроз головки бедренной кости (АНГБК).
Асептический некроз головки бедренной кости (АНГБК) – частое осложнение травм тазобедренного сустава с повреждением сосудов. Однако, чаще АНГБК имеет нетравматическое происхождение и первопричина заболевания остается неизвестной. В настоящее время доминирует теория полиэтологичности идиопатического АНГБК, которая подразумевает негативное действие факторов риска, таких как хронический алкоголизм, гиперлипидемия, курение, коагулопатии и ряд системных заболеваний [1]. Ряд авторов предполагают в качестве причинного фактора нарушение коагуляции, кровоснабжения и повторные травмы [2]. Помимо этого, установлены некоторые гены, связанные с развитием нетравматического АНГБК, а именно мутация гена COL2A1, кодирующего один из компонентов коллагена типа II [3]. Имеются и мутации, ассоциированные с АНГБК и гиперкоагуляцией – это так называемая Лейденовская мутация, дефект V плазменного фактора свертывания, который приводит к спонтанному образованию венозных тромбов [4]. Недавние исследования также показали взаимосвязь грелина, фактора фон Виллебранда и АНГБК. У пациентов с идиопатическим остеонекрозом значимо снижен уровень грелина и повышено значение фактора фон Виллебранда [5].
Перечисленные выше причины гиперкоагуляции невозможно выявить и учесть перед операцией эндопротезирования у каждого пациента. В научной литературе также отсутствуют данные об изменениях лабораторных показателей свертываемости крови, таких как ПТИ, АПТВ, концентрация фибриногена у пациентов с идиопатическим АНГБК.
Таким образом, идиопатический остеонекроз головки бедренной кости может сопровождаться предшествующим фоновым изменением коагулограммы в сторону гиперкоагуляции. Нанесение операционной травмы во время тотального эндопротезирования тазобедренного сустава может усугубить картину свертываемости крови и привести к еще более значимой гиперкоагуляции. Предполагается, что у пациентов с переломом шейки бедренной кости изменения коагулограммы носят менее значимый характер, поэтому данные пациенты были взяты за группу контроля.
Цель: сравнить изменения коагулограммы у пациентов с переломом шейки бедра с группой пациентов с коксартрозом и АНГБК после операции эндопротезирования тазобедренного сустава.
Материал и методы. В ретроспективный анализ включались пациенты после тотального эндопротезирования тазобедренного сустава в условиях спинномозговой анестезии. Всем пациентам были проведены исследования свертывающей системы крови, включающие следующие показатели: протромбиновое время (ПВ), протромбиновый индекс (ПТИ), активированное парциальное тромбопластиновое время (АПТВ), а также содержание фибриногена (ФГ) и тромбоцитов (PLT) в крови. Анализы проводились в течение 1 суток до операции и 6 суток после операции. Статистическая обработка проводилась в пакете Statistica 12. Статистическая значимость определялась с помощью U-критерия Манна-Уитни, значимыми считались различия при p<0,05.
Результаты.
В исследование включены 37 пациентов, из них с диагнозом перелом шейки бедренной кости – 14 пациентов, а с коксартрозом и асептическим некрозом головки бедренной кости (АНГБК) – 23 пациента. Средний возраст составил 60 лет. Профилактика тромбоэмболических осложнений у всех пациентов проводилась с помощью прямых ингибиторов Xa-фактора ривароксабана и апиксабана в профилактических дозах. Препараты назначались до операции и после операции в соответствии со стратификацией риска. Помимо этого, использовалось тугое эластическое бинтование нижних конечностей. Результаты коагулограммы представлены в таб. 1 и 2 и на рис. 1 и 2.
Таблица 1. Результаты коагулограммы у пациентов с АНГБК.
|
Анализ крови |
До операции |
После операции |
p |
|
ПТИ, % |
94,6 |
97,4 |
0,000 |
|
ПВ, с |
14,1 |
13,2 |
0,000 |
|
ФГ, г/л |
4,0 |
6,7 |
0,000 |
|
АПТВ, с |
30,2 |
28,8 |
0,060 |
|
PLT, кл*109/л |
245,4 |
267,8 |
0,520 |
Таблица 2. Результаты коагулограммы у пациентов с переломом шейки бедренной кости.
|
Анализ крови |
До операции |
После операции |
p |
|
ПТИ, % |
91,2 |
94,1 |
0,088 |
|
ПВ, с |
14,5 |
14,2 |
0,237 |
|
ФГ, г/л |
4,2 |
5,7 |
0,008 |
|
АПТВ, с |
32,3 |
33,9 |
0,752 |
|
PLT, кл*109/л |
231,4 |
245,4 |
0,548 |
Рисунок 1. Результаты коагулограммы у пациентов с АНГБК.
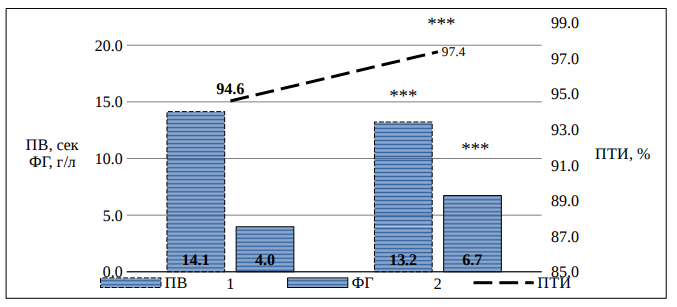
Примечание: *** - p<0,001.
Рисунок 2. Результаты коагулограммы у пациентов с переломом шейки бедренной кости.
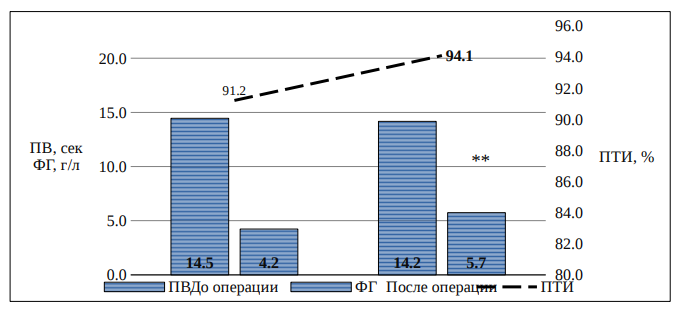
**
Примечание: ** - p<0,01.
До операции при сравнении обоих групп пациентов имеется лишь незначительная разница в значении ПТИ (p=0,035), однако после операции разница становится выражена. В группе АНГБК отмечается более значимая гиперфибриногенемия (p=0,015), чем в группе с переломом. Также меньшие значения ПВ (p=0,006) и АПТВ (p=0,025) и, соответственно, больший показатель ПТИ (p=0,007). Такая разница возникает по причине разной динамики анализов крови у разных групп пациентов. У пациентов с АНГБК отмечается статистически значимое увеличение фибриногена в крови, ПТИ и ускорение ПВ. В группе с переломом шейки бедра отмечается лишь увеличение фибриногена.
Выводы. Операция эндопротезирования тазобедренного сустава сопровождается более выраженным увеличением свертываемости крови у пациентов с асептическим некрозом бедренной кости и с коксартрозом, по сравнению с пациентами с переломом шейки бедра. Пациенты с АНГБК и с коксартрозом требуют более пристального внимания в отношение возможности развития тромбоза глубоких вен голени и тромбоэмболических осложнений.
Список литературы.
1) Коваленко А. Н., Ахтямов И. Ф. Этиология и патогенез асептического некроза головки бедренной кости. Генийортопедии. 2010. №2.
2) Hailer Y. D., Montgomery S., Ekbom A., Nilsson O., Bahmanyar S. Legg-Calve-Perthes disease and the risk of injuries requiring hospitalization: a register study involving 2579 patients // Acta Orthop. 2012. №83. С. 572–576.
3) Al-Omran A. K., Sadat-Ali M. Legg-Calve-Perthes disease in two generations of male family members: a case report // J Orthop Surg. 2013. №21. С. 258–261.
4) Woratanarat P., Thaveeratitharm C., Woratanarat T., Angsanuntsukh C., Attia J., Thakkinstian A. Meta-analysis of hypercoagulability genetic polymorphisms in Perthes disease // J Orthop Res. 2014. №32. С. 1-7.
5) Li C., Shen L., Yang Y., Shuai B., Xu X., Ma C. Plasma ghrelin and von Willebrand Factor levels in patients with non-traumatic osteonecrosis of the femoral head // Hip Int. 2015. №25. С. 76-81.
6) Geerts W.H., Pineo G.F., Heit J.A., Bergqvist D., Lassen M.R., Colwell C.W., Ray J.G. Prevention of venous thromboembolism: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy // Chest. 2004. №3. С. 338-400.
7) Heit J. A. Venous thromboembolism: disease burden, outcomes and risk factors // Journal of Thrombosis and Haemostasis. 2005. №3. С. 1611-1617.

















